Von: Redaktion HHU
Multiple Sklerose: Endogenes Retrovirus HERV-W maßgeblich an Schädigung des Nervengewebes beteiligt
Multiple Sklerose (MS) ist eine Autoimmunerkrankung des Zentralnervensystems (ZNS), die das Gehirn und Rückenmark betrifft. Ein Düsseldorfer Forscherteam um Prof. Dr. Patrick Küry von der Klinik für Neurologie hat zusammen mit Kollegen aus den USA und Kanada einen neuen Schädigungsweg des Nervengewebes durch ein endogenes Retrovirus entdeckt. Die Ergebnisse veröffentlichten sie nun in der Fachzeitschrift Proceedings of the National Academy of Sciences of the United States of America (PNAS).
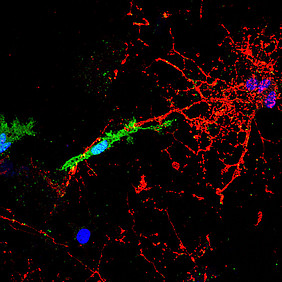
Frühe Krankheitsstadien der MS werden in erster Linie dadurch gekennzeichnet, dass Immunzellen das ZNS infiltrieren. Dies löst Entzündungen aus, die die sogenannten Myelinscheiden schädigen. Hierbei handelt es sich um elektrisch isolierende Strukturen, die durch bestimmte Gliazellen des ZNS – den sogenannten Oligodendrozyten – gebildet werden. Diese Strukturen schützen, ernähren und stabilisieren die Axone, die als Fortsätze der Neuronen elektrische Signale zu anderen Neuronen weiterleiten.
Zur Behandlung der MS steht eine Reihe von Medikamenten zur Verfügung, welche die entzündlichen Aspekte der sogenannten schubförmigen MS (relapsing MS; RMS) wirksam therapieren. Die neurodegenerativen Schäden, die bei Fortschreiten der Krankheit jedoch dominieren und zu nicht wiederherstellbaren Defiziten und anhaltender Behinderung führen, können trotz jahrzehntelanger intensiver Forschung noch nicht behandelt werden. Es gibt keine Therapien, die Schäden verhindern oder verletzte Axone reparieren können.
Ein Forschungsteam um Prof. Dr. Patrick Küry von der Klinik für Neurologie (Leitung Prof. Dr. Hans-Peter Hartung) hat zusammen mit Kollegen aus Cleveland (USA) und Montreal (Kanada) in einer kürzlich in PNAS veröffentlichten Studie einen neuartigen Schädigungsmechanismen identifiziert, der die Axone betrifft. Dieser kann möglicherweise für Patienten mit progressiver MS (PMS) von hoher Relevanz sein.
Sie stellten fest, dass das Hüllprotein (ENV) des pathogenen humanen endogenen Retrovirus Typ W (pHERV-W) maßgeblich bei der MS das Nervengewebe schädigt. PD Dr. David Kremer, Erstautor der Studie: „Das ENV-Protein bringt Mikrogliazellen im ZNS dazu, myelinisierte Axone anzugreifen und zu schädigen.“
Parallel zur wissenschaftlichen Aufklärung des Schädigungsmechanismus werden auch klinisch-therapeutische Entwicklungen, die das schädigende ENV-Protein bei MS Patienten neutralisieren können, vorangetrieben. Bereits in zwei klinischen Studien unter Leitung von Prof. Hartung wurde der ENV-neutralisierende Antikörper Temelimab dazu erfolgreich getestet. MRT-Aufnahmen der behandelten Studienteilnehmer zeigten eine verminderte Schädigung des Nervengewebes.
Die Düsseldorfer Forscher und ihre Kollegen können somit erklären, warum die Neurodegeneration bei Patienten abnimmt, die mit Temelimab behandelt wurden: Der Antikörper bindet spezifisch an das ENV-Protein des Retrovirus und blockiert seine Aktivität im ZNS. Prof. Hartung, Koautor PNAS- Publikation: „Künftige klinische Studien bei progressiven MS-Patienten müssen nun zeigen, ob die Behandlung mit Temelimab auch die klinischen Symptome der MS, die in Folge von Neurodegeneration auftreten, verbessern kann.“
Originalpublikation
Kremer D, Gruchot J, Weyers V, Oldemeier L, Göttle P, Healy L, Ho Jang J, Kang T Xu Y, Volsko C, Dutta R, Trapp BD, Perron H, Hartung HP, Küry P., pHERV-W envelope protein fuels microglial cell-dependent damage of myelinated axons in multiple sclerosis, Proc. Natl. Acad. Sci. U. S. A. 2019 Jun 18. pii: 201901283 PubMed
Quelle: UKD (Copyright 2019)


