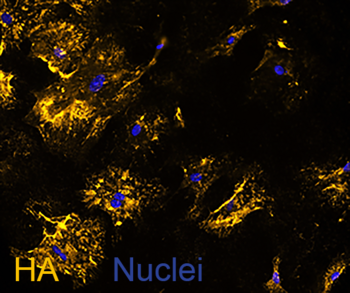
Microenvironment/extrazelluläre Matrix (EZM)
Kardiale Fibroblasten sind hochsynthetische Zellen und die Hauptproduzenten von EZM-Komponenten wie Kollagen Typ I und III, Fibronektin, Proteoglykanen (z.B. Versican, Biglykan oder Decorin) und Glykosaminoglykanen (v.a. Hyaluronsäure (HA)). Die Zusammensetzung, Struktur und Funktion der von Fibroblasten produzierten EZM sowie deren Wechselwirkung mit dem zellulären Microenvironment ist ein zentraler Forschungsschwerpunkt unserer Arbeitsgruppe.
Fokale Adhäsionen
Fokale Adhäsionen (auch Fokalkontakte oder Adhäsionsplaques genannt) sind spezielle, verankernde Kontaktstellen, die das Aktin-Zytoskelett einer Zelle mechanisch mit der extrazellulären Matrix (EZM) verbinden. Sie bestehen aus komplexen Proteinnetzwerken, wobei Integrine als zentrale Membranproteine fungieren, die auf der Zellaußenseite an EZM-Proteine binden und auf der Innenseite über Adapterproteine wie Talin, Vinculin, α-Actinin und Paxillin mit den Aktinfilamenten des Zytoskeletts verknüpft. Fokale Adhäsionen sind nicht nur für die mechanische Verankerung der Zelle an ihrer Umgebung verantwortlich, sondern spielen auch eine zentrale Rolle bei der Signalübertragung. Sie informieren die Zelle über den Zustand der EZM und beeinflussen so Zellverhalten, Wachstum, Überleben und Migration.
Genexpression
Zur Messung der mRNA-Expression von Differenzierungs- und Aktivierungsmarkern wie Acta2, Periostin oder Cthrc1 wird die RealTime-qPCR eingesetzt.
Hyaluronsäure-Coat
Hyaluronsäure ist ein langkettiges Polysaccharid, das zusammen mit Proteoglykanen einen wichtigen Bestandteil der EZM bildet und in die viele Zellen eingebettet sind. Die Ausbildung eines perizellulären HA-Coats erfolgt durch die HA-Synthese mittels drei unterschiedlicher HA-Synthasen, wobei HA über spezifische Rezeptoren wie CD44 an der Zellmembran verankert wird. Der Coat ist dynamisch, das heißt, seine Ausprägung kann je nach Zelltyp und physiologischer Situation variieren. Er schützt die Zelle vor mechanischem Stress, reguliert die Interaktion mit der Umgebung und spielt eine wesentliche Rolle bei der Zell-Zell-Kommunikation.
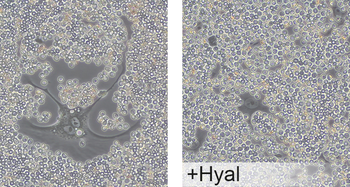
Particle exclusion assay
Der Erythrocyte Exclusion Assay ist ein zellbiologischer Test, der zur Visualisierung und Quantifizierung des perizellulären HA-Coats an Zellen eingesetzt wird. Das Prinzip beruht darauf, dass intakte Erythrozyten aufgrund ihrer Größe und fehlender Penetrationsfähigkeit nicht in die dichte HA-Schicht eindringen können. Im Assay werden Erythrozyten zu den zu untersuchenden Zellen gegeben. Die HA-Schicht wirkt als Barriere, sodass die Erythrozyten einen Abstand zur Zellmembran einhalten und einen „Ausschlussbereich“ (exclusion zone) um die Zelle herum bilden. Dieser Bereich kann mikroskopisch sichtbar gemacht und vermessen werden. Die Größe der Ausschlusszone korreliert mit der Dicke und Dichte des perizellulären HA-Coats.
HA-Sekretion
Kardiale Fibroblasten sind in der Lage, große HA-Mengen zu synthetisieren und zu sezernieren. Die HA-Sekretion ist ein wichtiger Aspekt ihrer Funktion und kann durch pro-inflammatorische Stimuli wie IL-6 verstärkt werden, was für die Gewebeantwort nach Herzschädigung und für die Regulation von Immun- und Reparaturprozessen von zentraler Bedeutung ist.
HA-Größenverteilung
Die zellbiologischen Funktionen von HA hängen nicht nur von der HA-Menge, sondern auch von der Molekülgrösse ab. Durch die gezielte Spaltung der HA-Ketten in kleinere Fragmente (z.B. durch Hyaluronidasen bzw. Depolymerisation) entsteht ein individuelles Muster der HA-Grössenverteilung, welches mittels Gelelektrophorese und definierten HA-Standards in Zellüberständen quantifiziert werden kann.
Während hochmolekulare HA eher einen ruhenden Fibroblasten-Phänotyp fördert, können niedermolekulare und oligomere HA-Fragmente die Fibroblasten-Aktivierung verstärken. Somit ist die Untersuchung der HA-Grössenverteilung ein wichtiges Tool zur Aufklärung HA-assoziierter Signalwege in kardialen Fibroblasten.