
Die Arbeitsgruppen von Prof. Schott und PD Willenberg beschäftigen sich mich verschiedenen Aspekten der Diagnostik und Therapie des Phäochromozytoms. Hierzu gehören z.B. Studien zur Identifizierung möglicher Tumorantigen beim malignen Phäochromozytom als auch Studien zu parakrinen Mechanismen etc.

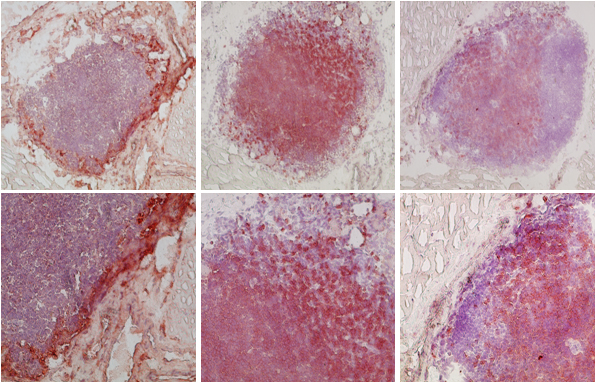 | 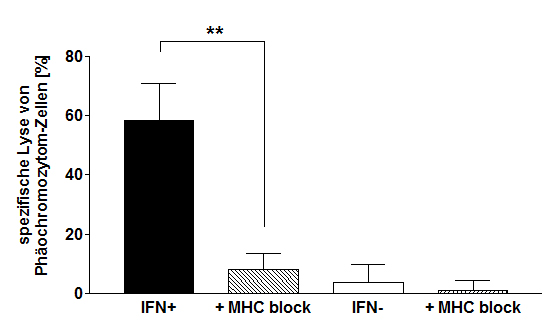 |
| In einer kürzlich von der Arbeitsgruppe von Prof. Schott publizierten Arbeit konnte weltweit erstmalig gezeigt werden, dass das neuroendokrine Tumorzell-spezifische Oberflächenmolekül Chromogranin A (CgA) auch als Tumorantigen fungiert. Auf der Basis eines Mausmodells konnte bewiesen werden, dass nach Immunisierung mit CgA-Peptiden eine CgA-spezifische Immunität induziert wird. Dies führt zur Infiltration von ex vivo applizierten Tumoren (Abbildung A) und eine Lyse von Tumorzellen durch aktivierte (Interferon gamma-sezernierende) T-Lymphozyten (Abbildung B). | |
Weitere Studien zum Phäochromozytom
Ausgangspunkte unserer Studien waren die Arbeiten der Arbeitsgruppe W. A. Scherbaum, in denen gezeigt werden konnte, dass Nebennierenmark und Nebennierenrinde sowohl morphologisch stark miteinander verwoben sind als auch funktionell durch parakrine Mechanismen interagieren.
So konnten wir und auch andere zeigen, dass chromaffine Phäochromozytomzellen in der Lage sind, ACTH autonom und in großen Mengen zu produzieren, sodass neben dem Katecholaminexzess in einer solchen Situation auch ein Glukokortikoidexzess auftritt, der klinisch bedeutsam ist.
Wir fanden außerdem, dass ein Nebennierenmarktumor und ein Nebennierenrindentumor prinzipiell gemeinsam auftreten können und diese für einen Katecholaminexzess neben einem bestehen Glukokortikoidexzess verantwortlich sind, sodass die Ursache eines gleichzeitig bestehenden Glukokortikoidexzesses nicht unbedingt im nachgewiesenem Phäochromozytom liegen muß. Andererseits könnte, entsprechend unserer Vorabeiten, in diesem Fall eine positive Rückkopplung zwischen beiden Tumoren stattgefunden haben, die durch Katecholamine und Glukokortikoide vermittelt wurde und auch Wachstumsreize für beide Gewebe beinhaltete. Dass dies auch praktisch möglich ist und der Zusammenhang nicht nur spekulativ hergestellt wurde, zeigt sich in einer aktuellen Veröffentlichung, in der beschrieben wurde, dass Phäochromozytomkrisen durch die Applikation von Glukokortikoiden ausgelöst werden können.
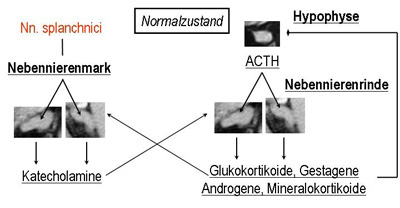 | Obere Abbildung: Nach Ausschüttung von CRH wird das sympathoadrenale System über die Nn. splanchnici aktiviert und im Nebennierenmark werden Katecholamine produziert. Diese verstärken die Synthese von Nebennierenrindenhormonen. Die Asschüttung von CRH führt auch zur Aktivierung der Hypophyse und nach Sekretion von ACTH zur Hormonproduktion in der Nebennierenrinde. Glukokortikoide und DHEA wirken auch auf die Synthese der Katecholamine ein. |
 | Mittlere Abbildung: Wenn ACTH ektop produziert wird, ist die Hormonsynthese in beiden Nebennierenrinden verstäkt. Über einen negativen Feedback führt das zur verminderten Synthese von ACTH in der Hypophyse. |
 | Untere Abbildung: Die vermehrte Produktion von Adrenalin in der einen Nebenniere und die vermehrte Produktion von Glukokortikoiden in der anderen verstärkt sich peripher gegenseitig. |
In experimentellen Arbeiten fanden wir eine differentielle Expression von Connexinen in den chromaffinen Zellen der Nebenniere. Dabei zeigte sich, dass sich normale adrenomedulläre Zellen und benigne Phäochromozytome durch eine höhere Expression von Connexin 50 von malignen Phäochromozytomen und Phäochromozytommetastasen unterscheiden.
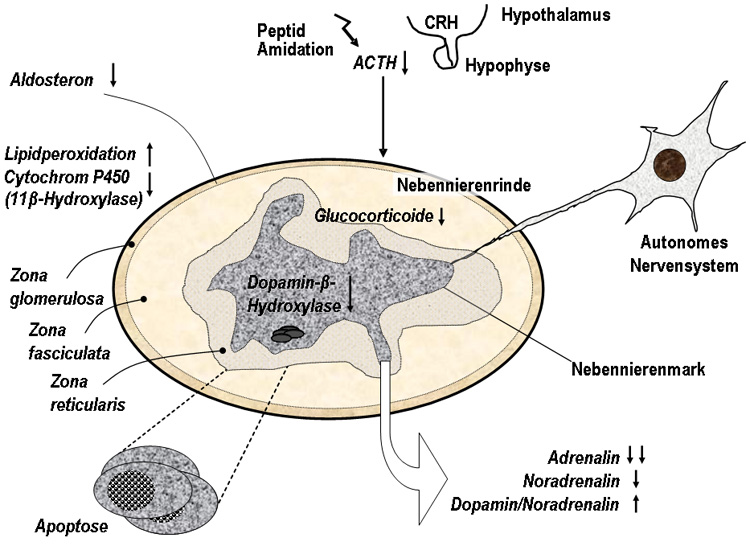
Dass Zell-Zell-Kontakte über Connexine zwischen chromaffinen Zellen für die Kommunikation der Zellen untereinander wichtig und auch ein Merkmal gutartiger Zellen sind, untersuchte Frau Dr. P. Patak in unserer Klinik. Wir stellten auch heraus, dass das Nebennierenmark sehr reich an Vitamin C ist und ein verminderter Transport von Vitamin C in die chromaffinen Zellen des Nebennierenmarks zu einer verminderten Katecholaminproduktion führt.
Ausgewählte Publikationen:
Ehrhart-Bornstein M, Hinson JP, Bornstein SR, Scherbaum WA und Vinson GP: Intraadrenal interactions in the regulation of adrenocortical steroidogenesis. Endocr Rev 1998, 19:101-143
Vrezas I, Willenberg HS, Mansmann G, Hiroi N, Fritzen R und Bornstein SR: Ectopic adrenocorticotropin (ACTH) and corticotropin-releasing hormone (CRH) production in the adrenal gland: Basic and clinical aspects. Microsc Res Techniq 2003, 61:308-314
Patak P, Willenberg HS und Bornstein SR: Vitamin C is an important co-factor for both adrenal cortex and adrenal medulla. Endocr Res 2004, 30(4):871-5
Wolf A, Willenberg HS, Cupisti K, Schott M, Geddert H, Raffel A, Bornstein SR, Scherbaum WA und Knoefel WT: Adrenal pheochromocytoma with contralateral cortisol-producing adrenal adenoma: diagnosic and therapeutic management. Horm Metab Res 2005, 37:391-395
Willenberg HS, Vrezas I und Bornstein SR: Störungen der neuro-, immuno- und endokrinen Regulation in der Nebenniere. In: Ganten, Ruckpaul & Köhrle (Eds.): Molekularmedizinische Grundlagen von para- und autokrinen Regulationsstörungen, 323-332. Springer, 2006
Willenberg HS, Feldkamp J, Lehmann R, Schott M, Goretzki PE und Scherbaum WA: A case of catecholamine-excess and Cushing''s syndrome due to a corticotropin-secreting paraganglioma. Ann N Y Acad Sci 2006, 1073:52-58
Willenberg HS, Schott M, Saeger W, Tries A, Scherbaum WA und Bornstein SR: Expression of connexins in chromaffin cells of normal human adrenals, benign and malignant pheochromocytomas.Ann N Y Acad Sci 2006, 1073:578-583
Rosas AL, Kasperlik-Zaluska AA, Papierska L, Bass BL, Pacak K und Eisenhofer G: Pheochromocytoma crisis induced by glucocorticoids: a report of four cases and review of the literature. Eur J Endocrinol 2008, 158:423-429


