AG Wesselborg: Signaltransduktion der Apoptose
Forschungsschwerpunkte:
- Signaltransduktion der Apoptose
- Chemoresistenzmechanismen bei Tumoren
Link zu "Vita Prof. Sebastian Wesselborg"
Programmierter Zelltod (Apoptose)
Der programmierte Zelltod spielt eine maßgebliche Rolle bei der embryonalen Morphogenese, der Elimination von Tumorzellen, virus-infizierten Zellen und autoreaktiven Thymozyten. Darüberhinaus stellt die Apoptose einen natürlichen Gegenspieler zur Zellproliferation dar und ist daher maßgeblich für die Aufrechterhaltung der Homöostase beim Zellumsatz verantwortlich. Es sind mittlerweile verschiedene Signalwege identifiziert worden, über die das endogene Selbstmordprogramm ausgelöst werden kann. Der sogenannte 'Todesrezeptorsignalweg' wird nach Bindung von natürlichen Liganden an Oberflächenrezeptoren wie CD95 (Fas, Apo-1) und den Rezeptoren für TNF und TRAIL ausgelöst. Der 'mitochondriale Apoptoseweg' wird über DNA-Schäden und zelluären Stress in der Zelle aktiviert. Beide Signaltransduktionswege aktivieren Proteasen der Caspase-Familie, welche durch proteolytische Spaltung von vitalen Zellproteinen zum Tod der Zelle führen.
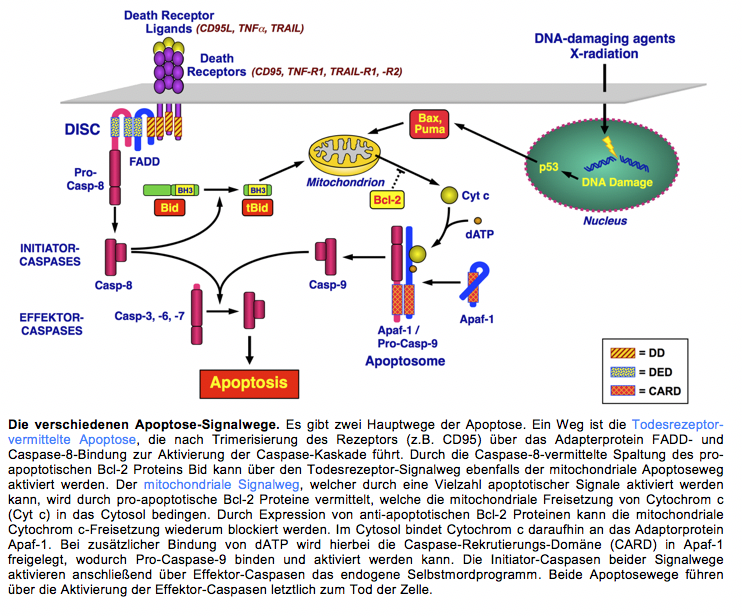
Signaltransduktion des programmierten Zelltods (Apoptose)
Da ein Hauptmechanismus der Radio- und Chemotherapie die Aktivierung des mitochondrialen Apotoseweges ist, ist es nicht verwunderlich, dass Tumore ihrerseits Resistenzen durch Inaktivierung des mitochondrialen Zelltodweges entwickeln. Am effektivsten erreichen Tumorzellen dies durch die Inaktivierung des Tumorsuppressors p53. Tumorzellen können aber auch pro-apoptotische Bcl-2 Proteine herunterregulieren und anti-apoptotische Bcl-2 Proteine hochregulieren oder wie im Falle von Melanomen, Glioblastomen und kolorektalen Tumoren Apaf‑1 epigenetisch herunterregulieren. Forschungsschwerpunkt der AG Wesselborg ist die Signaltransduktion der Apoptose. In diesem Zusammenhang haben wir uns in den letzten Jahren intensiv mit der molekularen Wirkungsweise der Apoptoseinduktion einer Reihe von pharmakologischen Agenzien (Chemotherapeutika, Kinaseinhibitoren, Prostaglandinen, Proteasominhibitoren, Mistellektinen, Tributylzinn und Naturstoffen) beschäftigt.
Chemoresistenzmechanismen bei Tumoren
Wir konnten erstmals zeigen, dass der Proteinkinase-Inhibitor Staurosporin in der Lage ist, in Zytostatika-resistenten Tumorzellen das endogene Selbstmordprogramm über einen bislang neuartigen intrinsischen Apoptose-Signalweg zu aktivieren. Wir untersuchen hierbei die Signaltransduktionswege von Staurosporin bei der Apoptose-Induktion mit dem Ziel der Entwicklung neuartiger Zytostatika, welche die Eliminierung von Tumoren ermöglichen, die bislang gegenüber konventionellen DNA-schädigenden Zytostatika resistent sind. Darüber hinaus sind wir u.a. im Rahmen des GRK 2158 an der Identifizierung neuartiger Signalwege interessiert, die unabhängig vom mitochondrialen Cytochrom c/Apaf-1-Weg Apoptose induzieren und damit die Eliminierung von therapieresistenten Tumorzellen ermöglichen.