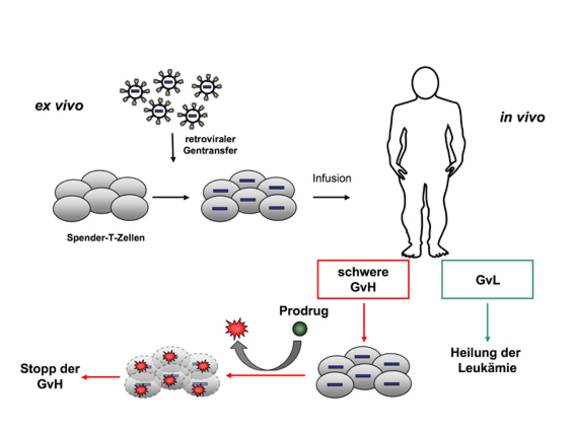
Suizidgentherapie
Für Patienten mit Rezidiven akuter und chronischer Leukämien nach allogener hämatopoetischer Stammzelltransplantation stellt die Infusion von reifen Lymphozyten des Stammzellspenders den einzigen noch potentiell kurativen Behandlungsansatz dar.
Diese so genannte donor-lymphocyte-infusion (DLI) ist allerdings wesentlich dadurch eingeschränkt, dass die immunkompetenten Zellen des Spenders nicht nur einen antileukämischen Graft-versus-Leukämie (GvL)-Effekt, sondern auch eine oft lebensbedrohliche Graft-versus-Host-Disease (GvHD) verursachen können.
Das wesentliche Problem hier ist: Je mehr T-Zellen verabreicht werden können, desto höher ist die Wahrscheinlichkeit, dass das Rezidiv erfolgreich behandelt werden kann. Gibt man zu wenige Zellen, stirbt der Patient am Rezidiv. Eine viel versprechende Maßnahme zur Kontrolle der GvHD stellt die Ausstattung der Spenderlymphozyten mit einem Suizidgen dar. Die Suizidgenprodukte überführen eine nicht-toxische Substanz (Prodrug) spezifisch in den Suizidgen-positiven Zellen in einen zytotoxischen Metabolit. Im Falle einer lebensgefährlichen GvHD lassen sich so die Suizidgen-tragenden Spenderlymphozyten selektiv durch die Applikation des Prodrugs eliminieren und die GvHD wird gestoppt.
Dieses Prinzip hat sich in klinischen Studien mit der Thymidinkinase vom Herpes Simplex Virus Typ 1 (HSV-tk) und Ganciclovir (GCV) als Prodrug prinzipiell als klinisch einsetzbar erwiesen. Allerdings ist das HSV-tk-Protein stark immunogen und führt häufig bei Expression in Spenderlymphozyten zur vorzeitigen immunvermittelten Eliminierung der Zellen. In unserer Arbeitsgruppe wird ein alternatives, aber humanes Suizidgensystem entwickelt, welches eine effiziente und spezifische Eliminierung der transgenen T-Lymphozyten ermöglicht. Für den Gentransfer in Spender-T-Lymphozyten nutzen wir lenti- oder foamyvirale Vektoren.
Damit liegt ein weiterer Forschungsschwerpunkt in der Etablierung eines effizienten viralen Vektorsystems für die klinische Anwendung in T-Zellen.